随着国家鼓励抗癌药物投放,加快靶向治疗和免疫治疗的审批程序,多种相关肿瘤治疗药品和生物标志物被相继开发,肿瘤个体化研究显示部分患者明显受益,以上因素都加快了国内癌症伴随诊断的行业发展。
而就在今年6月,2家肿瘤基因检测公司相继成功登陆纳斯达克,也让我们看到了在肿瘤NGS领域深耕多年后,中国基因检测企业终于迎来了高光时刻。
从2019年CMDE发布《肿瘤相关突变基因检测试剂(高通量测序法)性能评价通用注册技术审查指导原则》,到2020年中检院发布肿瘤突变负荷TMB检测国家参考品,着手NGS肿瘤相关突变基因检测试剂的标准化,监管的脚步伴随着行业发展一直在向前迈进。
本文以下内容由美国首款NGS测序仪Illuminia MiSeq的审查员Dr. Cheng Zhang独家授权法荟发布,带您了解FDA对肿瘤NGS的监管思路,未经本人及法荟允许请勿转发。
FDA监管整个IVD检测系统以及检测的每个组成部分,包括试剂,仪器和软件。NGS检测的定义是在特定的NGS仪器上按照工作流程(workflow)进行的核酸测序分析。工作流程中规定了全部使用的材料和程序,涵盖所有的步骤,例如样本类型、DNA提取、文库制备、测序、测序数据的计算处理,以及由系统检测出单个变异的临床意义的解释。具体来说,NGS 检测系统可以包括:
半岛体育 半岛官网
FDA对检测系统和其组成部分的监管在FDA首个NGS仪器授权中已经明确,FDA授权了IlluminaMiSeqDx 仪器及其通用测序试剂,以及2项用于诊断囊性纤维化的伴随检测(Illumina MiSeqDx 囊性纤维化139变异和临床测序分析)。下表列出了每种设备的监管途径。
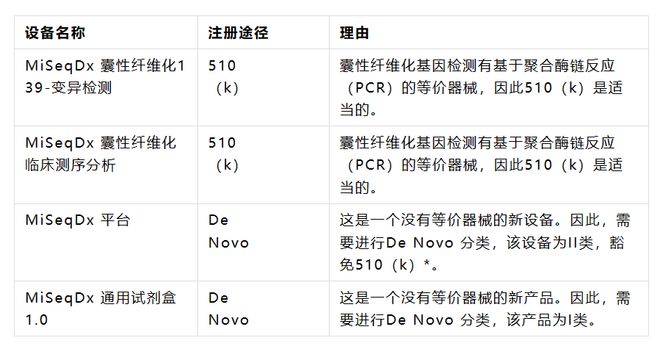
*豁免510(k)意味着即使它是II类设备,也不需要向FDA提交510(k)。
当FDA对IVD进行审查,以确定其是否符合适用的安全性和有效性要求,从而可以上市用于临床,FDA会审查该检测是否准确和可靠(分析验证)以及检测结果是否正确地识别了相关疾病或状态(临床验证)。
传统来讲,分析研究的所使用的是来源于目标适用人群的野生和变异临床样本。但是对于NGS panel,使用临床样品来验证panel中包括的所有变异是不切实际的。FDA认识到NGS panel分析验证中的挑战,并采用了更灵活的方法:
允许使用未经FDA许可/批准的检测(例如实验室开发的检测)作为比较方法,以证明NGS检测的准确性。
允许使用具有代表性的方法检测代表变异的一个子集,(例如具有代表性的SNV 单核苷酸变异,indels插入缺失,homopolymers同聚物,redundant sequences冗余序列等),而不是检测所有变异。
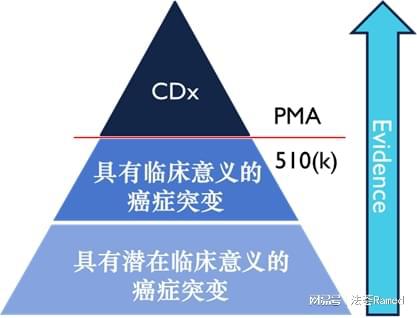
FDA对于NGS检测系统临床验证的要求取决于它的适用范围。FDA目前按照三等级方法来监管肿瘤NGS检测中的生物标志物。
肿瘤NGS检测可能包括针对特定治疗产品的CDx 声称。每种特定生物标志物检测的分析有效性和临床研究需要能够支持此类声称,该临床研究或者是建立了检测结果和患者结局之间的直接联系,或者证明了非原研CDx(follow-on CDx)与已批准的CDx 之间的临床一致性。
检测具有临床意义证据的癌症突变标志物,使医疗保健专业人员能够根据临床证据(例如,专业指南中提供的临床证据)恰当使用有关患者肿瘤的信息。开发人员可以通过证明检测对突变本身或代表性突变的分析有效性,以及基于可公开获得的临床证据(例如专业指南和/或经过同行评审的出版物)的临床验证为这类声称提供支持。
不能够被视为等级1或等级2生物标志物的突变可以描述为具有潜在临床意义的癌症突变。这些突变可能提供一些信息,或者用于指导患者参加可能符合其资格的临床试验。主要是通过证明检测对代表性突变的分析有效性,以及同行评审的出版物或体外临床前模型中涵盖的该类突变的临床或作用机理为这类声称提供支持。
经过FDA审查并批准的肿瘤NGS检测,开发人员可在产品上市后报告与初始递交中已经过分析验证的基因同类型的,并且与初始递交中建立的临床标准一致的其他变异,而无需向FDA提交新的申请。随着临床意义的证据被临床认可,并且只要在最初或后续的提交中审查并确定了检测的分析有效性,就可以将突变从3级转移到2级,而无需另外提交新的申请。

法荟(北京)医疗科技有限公司为国家高新技术企业,中国医疗器械行业协会临床试验分会副理事长单位。公司旨在为国内外医疗器械行业提供专业和规范的合规解决方案,帮助新产品和新技术的转化和上市。法荟于2020年成为康龙化成控股公司。法荟已为超过200+家国内外客户提供服务,团队拥有1000+ 成功案例的经验积累,可提供的服务涵盖从建立GMP厂房和管理体系、研发合规辅导,到全程临床试验、以及产品注册(包括驻场服务)。同时,法荟还可为医疗机构提供第三方稽查服务;为出口到美国的医疗器械产品提供美国FDA上市前许可服务;为和并购提供法规风险评估服务。
IVD注册信息荟享平台由康龙临床医疗器械部(法荟)倾力打造。平台以全面、及时、便捷、一站式的资讯检索方式,致力于为体外诊断行业提供专业的合规辅导。
特别声明:以上内容(如有图片或视频亦包括在内)为自媒体平台“网易号”用户上传并发布,本平台仅提供信息存储服务。
这张离谱的婚纱照在网上火了!网友无语吐槽:伴娘这胸,说不是故意的谁信??
印首位宇航员语出惊人:地球上有“外星人”,即那些为私利忽视人类共同命运的人
30艘军舰 120架战机 2.6万名官兵全部进入战备状态:这是针对谁?
美国一机器人展览会上连续工作20小时跪地倒下,网友调侃:机器人也会过劳死
半岛体育 半岛官网
网友回应“在浙大随手抓了两个院士帮拍照”:他们就像两位亲切的大叔,没架子
法荟专注于提供专业医疗器械(含体外诊断试剂)法规服务,致力于合规、高效地服务于患者健康.
6月发布,售价2万?苹果备战MR头盔,多款定制软件即将上线上海车展:汽车价格普遍下调,新能源已成常态
